기원
아르테미신의 역사와 잠재적인 치료 효과는 1967년 5월 23일 중국에서 항말라리아 약물 연구에 관한 국가 운영 그룹(National Steering Group)이 600개 이상의 연구소에 참여하여 항기생충 활성이 있는 새로운 활성 성분을 확인하기 위한 인상적인 검사를 시작했을 때 시작됩니다.

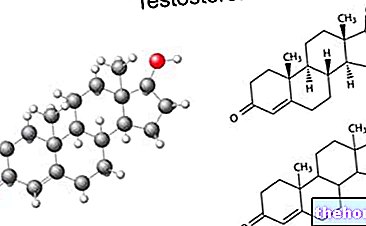
그림: 아르테미신의 화학 구조
불과 몇 년 후인 1972년경 한의학에서 전통적으로 사용하는 식물, 즉 "쑥쑥 - 아르테미신(Artemisin) 확인 복잡한 화학 구조를 가진 이 활성 성분은 약물 내성 기생충에도 항말라리아 작용을 발휘할 수 있음이 발견되었습니다.
1976년에 다양한 연구를 통해 아르테미신의 주요 작용 기전을 명확히 할 수 있었습니다. 특히, 이 산화된 세스퀴테르펜은 특정 엔도퍼옥사이드 구조 덕분에 철 이온과 상호작용하여 자유 라디칼을 형성하고 산화 쇼크로 인한 세포 사멸을 초래할 수 있습니다.
따라서 말라리아 플라스모디아 내부의 높은 농도의 철은 아르테미신 작용에 대한 이러한 기생충의 특정 민감성을 정당화합니다.
참고: Artemisin은 qinghaosu라고도 합니다.
치료적 관점
암세포는 또한 세포 내 철 이온 농도가 높으며 트랜스페린에 대한 많은 수의 막관통 수용체(세포외 철을 포획하여 세포로 운반하는 데 필요)와 결합합니다.
철 이온은 실제로 신생물 세포를 구별하는 격렬한 유사분열 분열 속도를 지원하는 데 필요합니다. 당연하게도 트랜스페린에 대한 막횡단 수용체의 농도는 종양의 공격성과 완벽하게 상관됩니다.
철분의 중요한 농도로 인해 악성 세포는 이론적으로 아르테미신의 산화 촉진 효과에 더 민감하여 오히려 선택적으로 만듭니다.
이러한 증거와 이러한 가정에 기초하여 종양학에서 아르테미신 및 아르테수네이트 및 디히드로아르테미신(DHA)과 같은 보다 선택적 유도체의 사용이 몇 년 전에 시작되었습니다.
따라서 현재까지 이러한 활성 성분의 주요 치료 약속은 종양학적 및 면역학적 병리와 관련된 것으로 정확히 남아 있습니다.
항암 작용 메커니즘
아르테미신의 항암 효과에 대한 연구가 이 주제에 대해 발표된 연구의 증가에 의해 강조된 엄청난 추진력으로 인해 우리는 가설을 세울 수 있었고, 어떤 경우에는 분자 모델을 통해 이 활성 물질의 다양한 잠재적 작용 메커니즘을 확인할 수 있었습니다. 원칙
현재, 아르테미신 및 그 유도체의 항암 특성은 다음과 같은 요인에 의해 뒷받침되는 것으로 보입니다.
- "항증식 활성: 암세포를 구별하는 복제주기의 불균형한 활성을 조절할 수 있습니다. 특히, 이러한 활성 원리는 증식 과정의 진행에 관여하는 사이클린 및 관련 키나제의 발현을 제어하는 것으로 보입니다.
따라서 이 모든 것은 세포 증식의 정지를 초래할 것입니다. - "프로아폽토시스 활성: 여러 암종 세포주에서 관찰된 바와 같이. 보다 정확하게는 아르테미신이 특히 고용량으로 사용되는 경우 세포자멸사 촉진 인자의 활성화를 유도하여 DNA 단편화 및 이에 따른 세포 사멸과 관련된 생물학적 메커니즘의 활성화를 결정할 수 있습니다.
- "항전이 활성: 종양 발달의 초기 단계에서 발생하는 미세 전이에 특히 중요합니다. 이러한 유형의 작용은 세포외 기질에 대한 종양 세포의 부착에 관여하는 인테그린 계열에 속하는 메탈로프로테아제 및 기타 단백질의 발현을 억제하는 아르테미신의 능력과 관련이 있는 것으로 보입니다.
- "항혈관신생 활성: 초기 실험적 증거에서, VEGF 및 FGF와 같은 인자의 발현을 억제하는 아르테미신의 능력은 전통적으로 혈관신생 현상에 관여하는 것으로 나타났습니다. 보다 정확하게는, 이러한 인자는 종양 덩어리에 영양을 공급하고 종양 클론의 혈액 확산을 촉진하는 데 필요한 종양 내 및 종양 주변 혈관 구조의 형성을 촉진할 것입니다.
- "화학 요법 지원 활동: 흥미로운 증거는 고전적인 화학 요법에 아르테미신과 그 유도체를 추가하는 것이 치료의 종양 세포 독성 효과를 향상시킬 수 있음을 보여 주었지만, 특히 반응이 부적절한 병리학 또는 불행하게도 약물 내성 종양의 경우에, 그러나 이러한 활성은 아직 명확하지 않습니다.
연구
이와 관련하여 대부분의 연구는 아직 실험적이므로 대부분 세포주 또는 동물 모델에서 수행되지만, 현재까지 상당히 재현 가능한 작용 메커니즘 덕분에 데이터가 특히 유망합니다.
시험관 내 테스트: 여러 연구에서 비만 세포주와 쥐의 신장 선암종에 대한 아르테미신 및 그 유도체의 세포독성 활성이 입증되었습니다.
보다 정확하게는, 이들 세포주를 아르테미신과 함께 72시간 배양하면 분자 의학에 의해 입증된 바와 같이 세포 사멸 과정의 유도 및 세포 주기 정지를 통해 증식이 70-90% 억제되었습니다.
또한 아르테미신을 치료 분야에서 전통적으로 사용되는 고전적인 세포독성 및 화학요법 약물과 연관시켜 우수한 효과를 얻었습니다.
이러한 연구의 결과로 국립 암 연구소의 치료 개발 프로그램은 대장, 유방, 난소 및 중추 신경계 암종, 췌장, 폐, 흑색종 및 백혈병의 세포주에 대해서도 아르테미신 및 그 반합성 유도체의 억제 효능을 관찰했습니다. .
생체 내 시험 - 실험 모델: 시험관 연구의 성공으로 암과의 싸움에 종사하는 연구자들이 동물 암의 실험 모델에서도 아르테미신 및 그 유도체의 효능을 시험하게 되었습니다.
주로 고형 종양에 대해 수행된 이 연구에서 아르테미신의 섭취가 종양의 기하급수적인 성장을 유의하게 늦추어 임상 양상의 전반적인 개선뿐만 아니라 사망률의 현저한 감소로 이어지는 것으로 관찰되었습니다. . . .
임상 시험: Artemisin 및 그 유도체는 또한 인간 임상 시험 및 단일 임상 사례에서 사용되었습니다.후두의 편평 세포 암종, 뇌하수체 거대선종 및 일부 형태의 폐암에 대해 흥미로운 성공이 관찰되었습니다.
이 모든 연구에서 앞서 언급한 활성 성분이 고전적인 화학 요법에 추가되었습니다.
이러한 유도체의 실제 임상 잠재력을 이해하기 위한 많은 연구가 여전히 진행 중입니다.
아르테미신의 독성
아르테미신의 치료적 사용과 관련된 잠재적인 독성 효과를 확인할 수 있는 장기 연구는 아직 없지만, 첫 번째 실험 연구는 특히 고용량에서 주로 신경 독성 효과를 보여줍니다.
그러나 항말라리아제로 아르테미신을 사용하는 것과 관련하여 문헌에 발표된 연구를 참조하면 이 활성 성분은 표준 용량에서 잘 견디는 것으로 보입니다.
미래의 응용
Artemisin은 민감한 항말라리아 작용으로 이미 수년 동안 권장되었습니다.
그러나 이 활성 원리는 특히 강력한 세포 증식 억제 및 세포 독성 가능성에 대해 최근에 매우 효과적인 것으로 입증되었습니다.
실험 연구는 아르테미신 및 그 유도체의 높은 항종양 효능을 입증했으며, 특히 치료에 특히 공격적이거나 적절하게 반응하지 않는 종양에 대해 임상의에게 추가적인 치료 대안을 제공할 수 있습니다.
이러한 유망한 연구를 기반으로 하는 전체 과학적 파노라마는 현재 진행 중인 다양한 임상 시험이 수행된 치료 가설을 검증할 수 있기를 희망하며, 따라서 암과의 싸움에서 의사에게 유리하게 잠재적인 치료 선택을 확장할 수 있습니다.
서지
암 세포주에 대한 아르테미시닌의 차등 효과.
Tilaoui M, 마우스 HA, Jaafari A, Zyad A.
Nat Prod Bioprospect. 2014년 6월 4일: 189-96.
아르테미시닌 유도체 아르테수네이트는 시험관내 및 생체내 자궁경부암 세포에서 방사선 민감성을 유도합니다.
Luo J, Zhu W, Tang Y, Cao H, Zhou Y, Ji R, Zhou X, Lu Z, Yang H, Zhang S, Cao J.
라디에트 온콜. 2014년 3월 25일 9:84
시험관 내 및 생체 내에서 artesunate와 captopril에 의한 혈관 신생의 상승적 억제.
Krusche B, Arend J, Efferth T.
Evid Based Complement Alternat Med. 2013, 2013: 454783.
[아르테미시닌 및 그 유도체의 항종양 활성 연구 진전].
양 H, 탄 XJ.
Zhongguo Yi Xue Ke Xue Yuan Xue Bao. 2013년 8월 35일: 466-71
아르테미시닌은 인간 암세포에서 세포자멸사를 유도합니다.
싱 NP, 라이 HC.
Anticancer Res. 2004 Jul-Aug, 24: 2277-80.
Dihydroartemisinin은 난소암 세포 성장의 억제제입니다.
Jiao Y, Ge CM, Meng QH, Cao JP, Tong J, Fan SJ.
Acta Pharmacol 신. 2007년 7월 28일: 1045-56
아르테미시닌 및 그 유도체의 항종양 활성: 잘 알려진 항말라리아제부터 잠재적인 항암제까지.
Crespo-Ortiz MP, Wei MQ.
J Biomed Biotechnol. 2012, 2012: 247597
디하이드로아르테미시닌(DHA)은 인간 폐 선암종 ASTC-a-1 세포에서 카스파제-3 의존성 세포자멸사를 유도합니다.
Lu YY, Chen TS, Qu JL, Pan WL, Sun L, Wei XB.
J Biomed Sci. 2009년 2월 2일, 16: 16