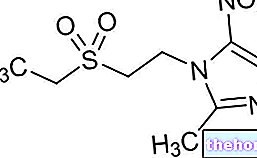
Ristempa는 무엇이며 무엇에 사용됩니까?
리스템파는 암 환자가 치료의 일부 부작용을 완화하기 위해 사용하는 약입니다. 세포 독성(즉, 세포 파괴)인 화학 요법(항암 치료)은 백혈구도 죽입니다. 이것은 호중구 감소증(감염과 싸우는 백혈구의 일종인 낮은 수준의 호중구) 및 감염의 발병으로 이어질 수 있습니다. Ristempa는 호중구감소증의 연장과 발열성 호중구감소증(즉, 발열과 결합된 호중구감소증)의 발병률을 감소시키는 데 사용됩니다. Ristempa는 만성 골수성 백혈병(백혈구에 영향을 미치는 암의 일종) 환자에게는 사용할 수 없습니다. 골수이형성증후군(백혈구의 과도하게 증가하여 백혈병을 유발할 수 있는 질환) 환자 리스템파는 활성물질인 pegfilgrastim을 함유하고 있으며, 이 약은 이미 유럽연합(EU)에서 승인된 Neulasta와 동일합니다. . . Neulasta의 제조업체는 과학적 데이터가 Ristempa에 사용될 수 있음을 인정했습니다("정보에 입각한 동의").
Ristempa는 어떻게 사용됩니까 - pegfilgrastim?
리스템파는 처방전이 있어야만 구할 수 있으며 암이나 혈액 질환 치료에 경험이 있는 의사가 치료를 시작하고 감독해야 합니다.
Ristempa는 6mg의 pegfilgrastim이 포함된 미리 채워진 주사기에 주사용 용액으로 제공됩니다. 각 화학요법 주기가 끝난 후 약 24시간 후에 6mg의 단일 피하 주사로 제공됩니다. 적절한 지시가 있으면 환자가 직접 주사를 투여할 수 있습니다.
Ristempa는 어떻게 작동합니까 - pegfilgrastim?
리스템파에 함유된 활성성분인 pegfilgrastim은 filgrastim으로 구성되어 있는데, 이는 granulocytic colony-stimulating factor(G-CSF)로 알려진 인간 단백질과 매우 유사한 "pegylated" 형태로 구성되어 있습니다. 폴리에틸렌 글리콜). Filgrastim은 골수를 자극하여 더 많은 백혈구를 생성하고, 백혈구 수를 증가시키며, 호중구 감소증을 치료함으로써 작용합니다. 유럽 연합(EU) 내에서 필그라스팀은 몇 년 동안 다른 의약품에서 사용 가능했습니다. pegfilgrastim에서 filgrastim은 pegylated 형태로 존재합니다. 이것은 신체의 약물 제거를 늦추므로 투여 빈도를 줄입니다.
연구 기간 동안 Ristempa - pegfilgrastim이 보여준 이점은 무엇입니까?
리스템파는 세포독성 화학요법으로 치료받은 총 467명의 유방암 환자를 대상으로 하는 두 가지 주요 연구에서 연구되었습니다. 두 연구에서 각각 4회의 화학요법 주기 동안 리스템파의 단일 주사 효과와 필그라스팀의 매일 여러 차례 주사 효과를 비교했습니다.효과의 주요 척도는 화학요법의 첫 번째 과정 동안 중증 호중구감소증의 지속 기간이었습니다. Ristempa는 중증 호중구 감소증의 기간을 줄이는 데 필그라스팀과 동등하게 효과적이었습니다. 두 연구 모두에서 환자는 화학요법의 첫 번째 과정 동안 약 1.7일 동안 심각한 호중구감소증을 앓았고, 두 약물이 없는 경우에는 약 5-7일의 간격을 보였습니다.
Ristempa - pegfilgrastim과 관련된 위험은 무엇입니까?
리스템파의 가장 흔한 부작용(10명 중 1명 이상에 영향을 미칠 수 있음)은 뼈와 근육통, 두통 및 메스꺼움입니다. 부작용 및 제한 사항의 전체 목록은 패키지 전단지를 참조하십시오.
Ristempa - pegfilgrastim이 승인된 이유는 무엇입니까?
FDA의 인체용 의약품 위원회(CHMP)는 Ristempa의 이점이 위험보다 크다고 결정하고 EU에서 사용 승인을 받을 것을 권장했습니다.
Ristempa - pegfilgrastim의 안전하고 효과적인 사용을 보장하기 위해 어떤 조치가 취해지고 있습니까?
Ristempa를 최대한 안전하게 사용할 수 있도록 위험 관리 계획이 개발되었습니다. 이 계획에 따라 리스템파의 제품 특성 요약 및 패키지 전단지에 의료 전문가와 환자가 따라야 할 적절한 예방 조치를 포함하여 안전 정보가 추가되었습니다. 추가 정보는 위험 관리 계획 요약에서 찾을 수 있습니다.
Ristempa에 대한 기타 정보 - pegfilgrastim
2015년 4월 13일, 유럽 위원회는 유럽 연합 전역에서 유효한 Ristempa에 대한 "판매 허가"를 발행했습니다.Ristempa 요법에 대한 자세한 내용은 패키지 전단지(EPAR에 포함됨)를 읽거나 의사 또는 약사에게 문의하십시오. 이 요약의 마지막 업데이트: 04-2015.
이 페이지에 게시된 Ristempa - pegfilgrastim에 대한 정보는 최신 정보가 아니거나 불완전할 수 있습니다. 이 정보를 올바르게 사용하려면 고지 사항 및 유용한 정보 페이지를 참조하십시오.